Antwort Jak poznat silnou a slabou zásadu? Weitere Antworten – Jak se určuje síla kyseliny
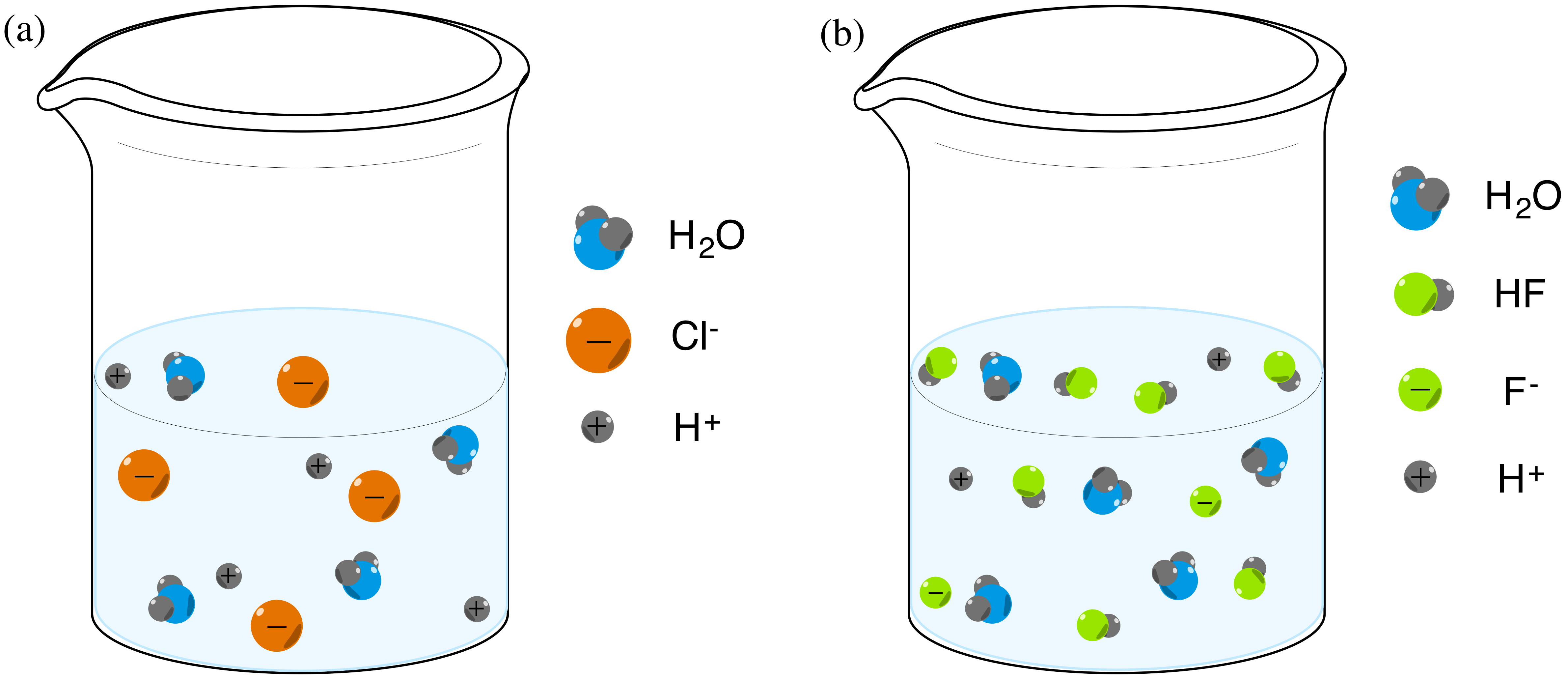
Sílu kyseliny definuje její disociační konstanta. Je to rovnovážná konstanta charakterizující protolytickou rovnováhu v roztoku a nazývá se disociační konstanta kyseliny KA.Za kyseliny jsou podle této teorie považovány látky, které ve svých roztocích jeví měřitelnou snahu odštěpovat své protony H+. V protikladu k tomu jsou za zásady označovány látky, které ve svých roztocích jeví měřitelnou snahu protony H+ přijímat.Slabé kyseliny jsou kyseliny, které disociují v roztoku pouze částečně. Jinými slovy je slabá kyselina jakákoliv kyselina, která není silnou kyselinou. Síla slabé kyseliny závisí na tom, do jaké míry probíhá disociace: čím více disociuje, tím silnější kyselina je.
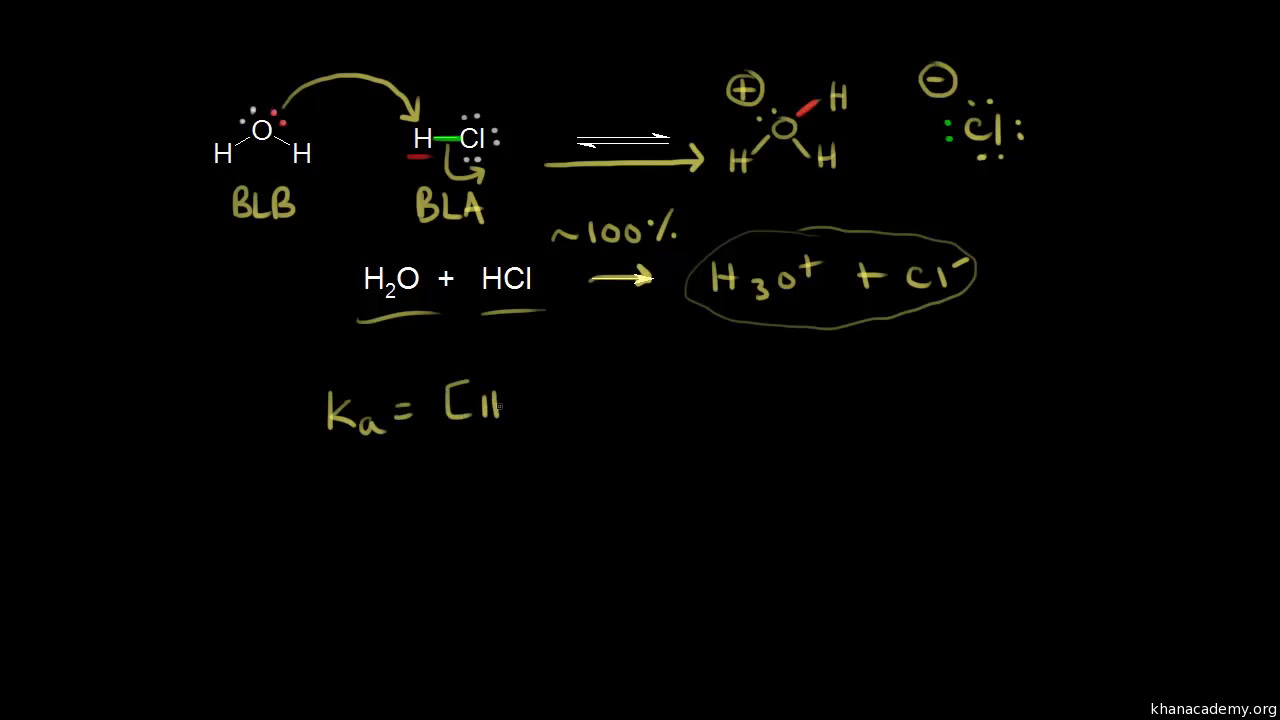
Jak poznat konjugovaný pár : Teď zavedeme pojem "konjugovaný pár" – to je dvojice látek (jedné kyseliny a jedné zásady), které se liší o ten jeden proton. Prvním konjugovaným párem je zde HCl a Cl-, protože je to jedna kyselina a jedna zásada a liší se o proton. Druhým konjugovaným párem je samozřejmě H2O a H3O+.
Jak poznam která kyselina je silnejsi
u kyslíkatých kyselin obecně platí, že nejslabší jsou ty, v jejichž molekulách se shoduje počet atomů H a O. Čím více je atomů O ve srovnání s H, tím je kyselina silnější (lze vysvětlit i indukčním efektem atomů kyslíku, který způsobuje kyselost vodíku).
Co to je pKa : Z obecné chemie víme, že pKa je rovno záporně vzatému dekadickému logaritmu z Ka. Čím nižší je hodnota pKa, tím silnější je daná kyselina. V organické chemii hodnotu pKa hojně využíváme. Z toho důvodu je dobré této veličině dobře porozumět.
Konstanta bazicity číselně popisuje sílu zásady. Čím je její hodnota vyšší, tím je zásada silnější. Koncentrace vody se téměř nemění, proto se zahrnuje do rovnovážné konstanty: Příklady silných zásad: KOH, NaOH, LiOH, Ba(OH)2,….
Sílu kyseliny posuzujeme podle toho, jak snadno se z ní odštěpí proton, sílu zásady podle toho, jak snadno proton váže.
Jak poznat silnou a slabou kyselinu
Kyselina je tím silnější, čím snadněji odštěpí H+, zásada je tím silnější, čím snadněji H+ váže. Čím je zásada (kyselina) silnější, tím slabší je její konjugovaná kyselina (zásada).Kyselina fluoroantimoničná
Co je zač: Nejsilnější kyselina na světě. Řadí se mezi tzv. superkyseliny.☑ Čím je hodnota Ka větší, tím je hodnota pKa menší. ☑ Čím je hodnota pKa větší, tím je hodnota Ka menší. ☑ Čím je hodnota pKa menší, tím je kyselina silnější. ☑ Čím je hodnota Ka menší, tím je hodnota pKa větší.
Příklady silných zásad: KOH, NaOH, LiOH, Ba(OH)2,…. Příklady slabých zásad: NH3, organické aminy, Al(OH)3,…..
Jak neutralizovat kyseliny : Kyselé roztoky lze neutralizovat zásaditými roztoky a naopak. Silné kyseliny vytvářejí oxoniové ionty H3O+ zcela rozpuštěné ve vodě s pH < 7, silné báze vytvářejí zcela rozpuštěné hydroxidové ionty OH− s pH > 7. V průběhu této reakce dochází ke změnám pH roztoku a dokonale neutralizovaný roztok má výsledné pH = 7.
Jak poznat sílu zásad : Kyselina je tím silnější, čím snadněji odštěpí H+, zásada je tím silnější, čím snadněji H+ váže. Čím je zásada (kyselina) silnější, tím slabší je její konjugovaná kyselina (zásada).
Čím se neutralizuje kyselina
Kyselé roztoky lze neutralizovat zásaditými roztoky a naopak. Silné kyseliny vytvářejí oxoniové ionty H3O+ zcela rozpuštěné ve vodě s pH < 7, silné báze vytvářejí zcela rozpuštěné hydroxidové ionty OH− s pH > 7. V průběhu této reakce dochází ke změnám pH roztoku a dokonale neutralizovaný roztok má výsledné pH = 7.
Je to silná jednosytná kyselina. Vzniká rozpuštěním plynného HCl (chlorovodíku) ve vodě. Reaguje s celou řadou neušlechtilých kovů (Fe, Zn, Al, Na …), za vzniku v kyselině chlorovodíkové rozpustných chloridů. S ušlechtilými kovy nereaguje.Nejsilnější zásada má pH 14. Neutrální látka má pH 7.
Co delat kdyz nekdo vypije kyselinu : Při požití kyselin a louhů nikdy nevyvoláváme zvracení! Postiženého necháme vypít větší sklenici vody a tím se snažíme snížit koncentraci chemické látky v trávicím ústrojí.