Antwort Jak se zaplňují orbitaly? Weitere Antworten – Jak jdou za sebou orbitaly
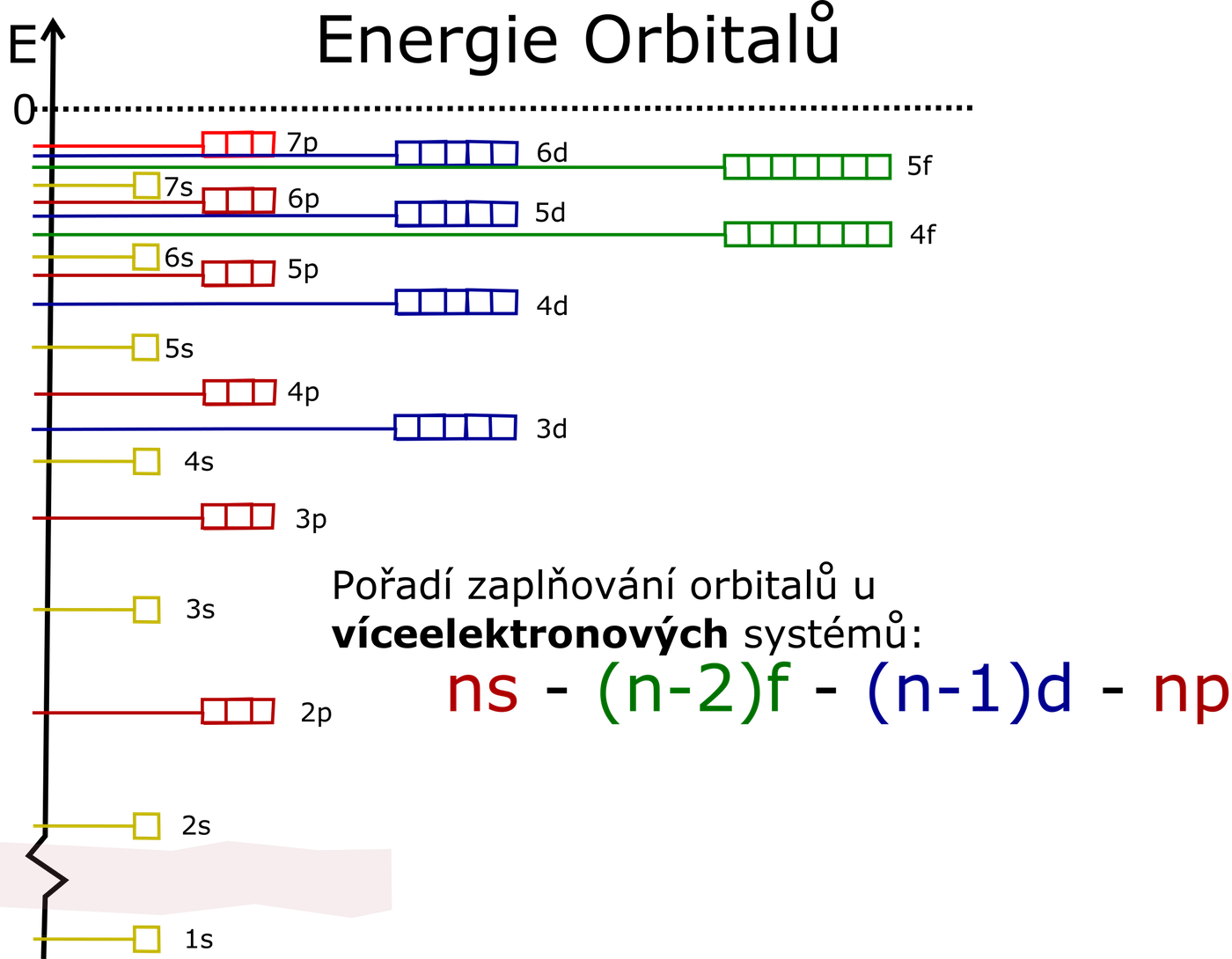
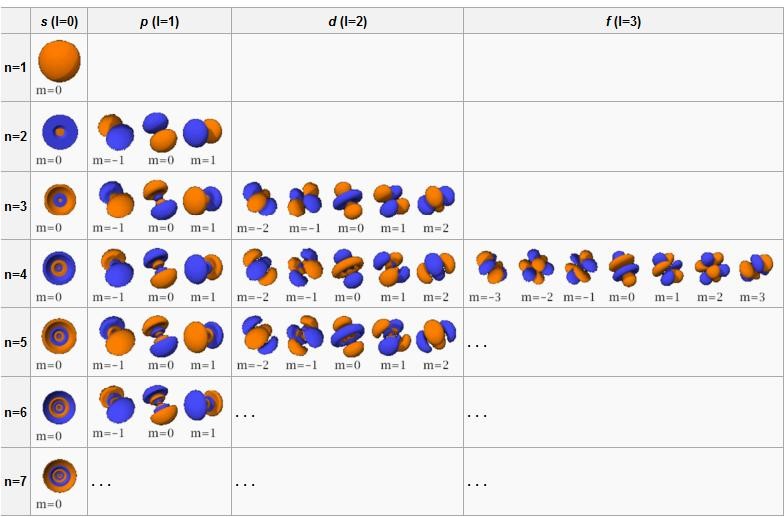
Orbitaly se obsazují podle rostoucí energie v pořadí: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p, … S tímto pořadím zcela koresponduje uspořádání prvků v periodickém systému.Orbital p (l = 1) má tvar dvou rotačně symetrických laloků, vzájemně středově symetricky vybíhajících od středu atomu do směru vybrané souřadné osy (v každém laloku má vlnová funkce jiné znaménko). Magnetické číslo může nabývat hodnot m = −1,0,1, orbital je tedy 3× degenerovaný.Jednoduše řečeno, elektronové obaly jsou úrovně se stejným hlavním kvantovým číslem n . Obálka nejvzdálenější od atomového jádra se nazývá valenční obal – elektrony obíhající po tomto obalu se nazývají valenční elektrony (vytvářejí chemické vazby mezi atomy různých prvků nebo atomy téhož prvku).
Kolik elektronů má orbital f : Do s-orbitalu se vejdou 2 elektrony, pro p-orbital to je 6, v d-orbitalu může být nejvýše 10 elektronů a v f-orbitalu jich najdeme nejvýše 14. Pořadí, ve kterém jsou tyto orbitaly zaplňovány, je přesně udáno výstavbovým principem.
Kolik atomových orbitalů je ve vrstvě N 2
v první periodě se nacházejí pouze dva prvky, tj. vodík a helium. Hlavnímu kvantovému číslu dvě odpovídají dvě hodnoty vedlejšího kvantového čísla (n = 2, l = 0 a 1). Druhá elektronová vrstva obsahuje orbitaly typu s a p, k jejichž úplnému zaplnění je třeba 8 (2 + 6) elektronů.
Jak zjistit počet elektronů : V neutrálním atomu je počet protonů stejný jako počet elektronů, a proto počet elektronů můžeme snadno určit z atomového čísla. Navíc pozice prvku v periodické tabulce—sloupec, skupina, řádek nebo perioda—poskytují užitečné informace o uspořádání elektronů ve slupkách.
Existencí tzv. vakantních orbitalů (→ orbitalů, jenž neobsahují elektrony, mají však stejné n jako zaplňené orbitaly) a dodáním energie lze vaznost zvětšit tím, že elektron vystoupí na vyšší energetickou hladinu (! stejné n, vyšší l). To dovoluje atomu poskytnout více nepárových elektronů a tím i větší vaznost.
je vnější část atomu obklopující atomové jádro. Obal atomu je tvořen elektrony a má záporný náboj.
Kolik elektronů je v obalu atomu
Různé atomy se liší svým složením: počtem jednotlivých částic. Atomy různých prvků se liší svým atomovým číslem, které vyjadřuje počet protonů v jádře (např. atom se šesti protony je atomem uhlíku; počet elektronů v obalu je u běžného elektricky neutrálního atomu shodný s počtem protonů v jádře).V orbitalu existuje jeden nebo dva elektrony. Atomy mohou mít i neobsazené orbitaly. Stav elektronu v obalu atomu se popisuje čtyřmi kvantovými čísly. Tři kvantová čísla charakterizují orbital, ve kterém je elektron, čtvrté kvantové číslo charakterizuje chování elektronu v orbitalu.Atom může mít 1 – 7 elektronových vrstev. Počet elektronů v jednotlivých vrstvách atomu je přesně stanoven. Rozmístění elektronů v elektronovém obalu (elektronová konfigurace atomu) určuje chemické vlastnosti prvků.
Atomy dosud známých prvků obsazují elektrony 7 elektronových vrstev, které se označují čísly 1 až 7 nebo písmeny K,L,M,N,O,P,Q. Maximální počet elektronů v každé vrstvě se rovná dvojnásobku počtu orbitalů, protože v jednom orbitalu mohou být maximálně dva elektrony.
Jaký počet elektronů má sodík : Každý prvek se snaží zcela zaplnit svou valenční slupku na maximální počet elektronů, tedy stejně jako ji mají zaplněnou prvky osmé skupiny – vzácné plyny. Na obrázku je příklad fluoru, který má ve valenční slupce sedm elektronů (červené body na valenční slupce), a sodíku, který má ve valenční slupce jeden elektron.
Kdo vymyslel orbital : Orbital Sciences Corporation
| Orbital Sciences | |
|---|---|
| Základní údaje | |
| Nástupce | Orbital ATK |
| Zakladatelé | David Thompson, Bruce Ferguson a Scott Webster |
| Sídlo | Dulles, Virginie, USA |
Co je to orbital
Orbital je trojrozměrný útvar (část prostoru). Záporně nabité částice elektronu, které jsou v obalu atomu, se rychle pohybují. Používá se zjednodušený model záporného náboje pro orbitaly. Oblast výskytu elektronu (orbital) není ostře ohraničena.
Orbital atomový
vymezují jakousi existenční oblast elektronu v atomu. Této oblasti nejpravděpodobnějšího výskytu elektronu se říká atomový orbital. Atomové orbitaly se označují symbolem obsahujícím hlavní kvantové číslo n a písmeno, které odpovídá hodnotě vedlejšího kvantového čísla l.protonové (atomové) číslo Z – je rovno počtu protonů v jádře, udává také počet elektronů obíhajících kolem jádra.
Jak zjistit počet orbitalů : Uvedeme nejdřív hlavní kvantové číslo, potom symbol vedlejšího kvantového čísla a na závěr počet elektronů (píšeme jako exponent). Rámečky obsahují tolik políček, kolik orbitalů příslušného typu existuje.