Antwort Kolik je elektronů v orbitalu? Weitere Antworten – Kolik elektronů se vejde do orbitalu
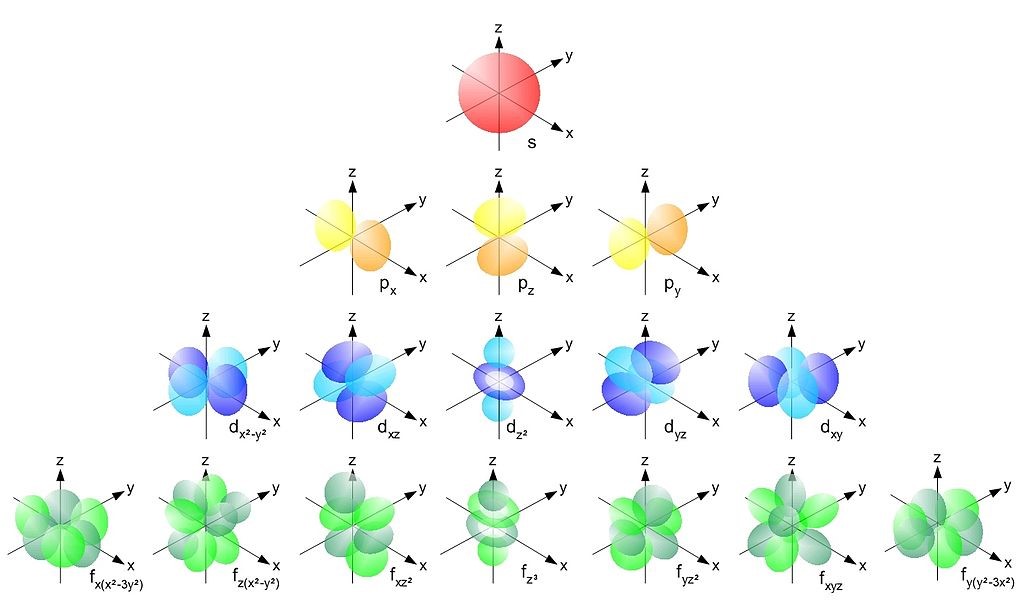
Důležitou informací pro nás bude, kolik elektronů se vejde do každé "slupky" kolem atomu. Do s-orbitalu se vejdou 2 elektrony, pro p-orbital to je 6, v d-orbitalu může být nejvýše 10 elektronů a v f-orbitalu jich najdeme nejvýše 14. Pořadí, ve kterém jsou tyto orbitaly zaplňovány, je přesně udáno výstavbovým principem.protonové (atomové) číslo Z – je rovno počtu protonů v jádře, udává také počet elektronů obíhajících kolem jádra.Za normálních okolností je počet elektronů v obalu stejný jako počet protonů v jádře – atom je navenek elektricky neutrální. Atom určitého chemického prvku má (podle pořadí prvku v Mendělejevově tabulce) v obalu určitý počet elektronů a v jádře stejný počet protonů.
Co je to orbital : Orbital je trojrozměrný útvar (část prostoru). Záporně nabité částice elektronu, které jsou v obalu atomu, se rychle pohybují. Používá se zjednodušený model záporného náboje pro orbitaly. Oblast výskytu elektronu (orbital) není ostře ohraničena.
Kolik orbitalů se nachází v elektronové vrstvě N 3
Spinové kvantové číslo m s
| Kvantové číslo | Poznámka | |
|---|---|---|
| hlavní n | vedlejší l | |
| 3 | 1 | ve sféře jsou 3 orbitaly p |
| 2 | ve sféře je 5 orbitalů d | |
| 4 | 0 | ve sféře je 1 orbital s |
Jak se zaplňují orbitaly : Pravidlo : Orbitaly se zaplňují v pořadí rostoucí hodnoty součtu . Pokud je možno stejné hodnoty dosáhnout více způsoby, např. obsazuje se napřed orbital s nižším hlavním kvantovým číslem (v tomto případě orbital 3d).
Počet valenčních elektronů
| Pořadí | Prvek | Valenční elektrony |
|---|---|---|
| 1 | Vodík | 1s1 |
| 2 | Helium | 1s2 |
| 3 | Litium | 2s1 |
| 4 | Berylium | 2s2 |
V jádře atomu sodíku se nachází 11 protonů a v obalu 11 elektronů. Zaokrouhlením hmotnostního čísla 22,99 do čísla celého, vyjde 23. Počet neutronů v jádře atomu sodíku se rovná: 23 – 11 = 12. Číslo periody v periodické tabulce ukazuje do kolika vrstev jsou roztříděny všechny elektrony v atomech této periody.
Jak se zaplňují Orbitaly
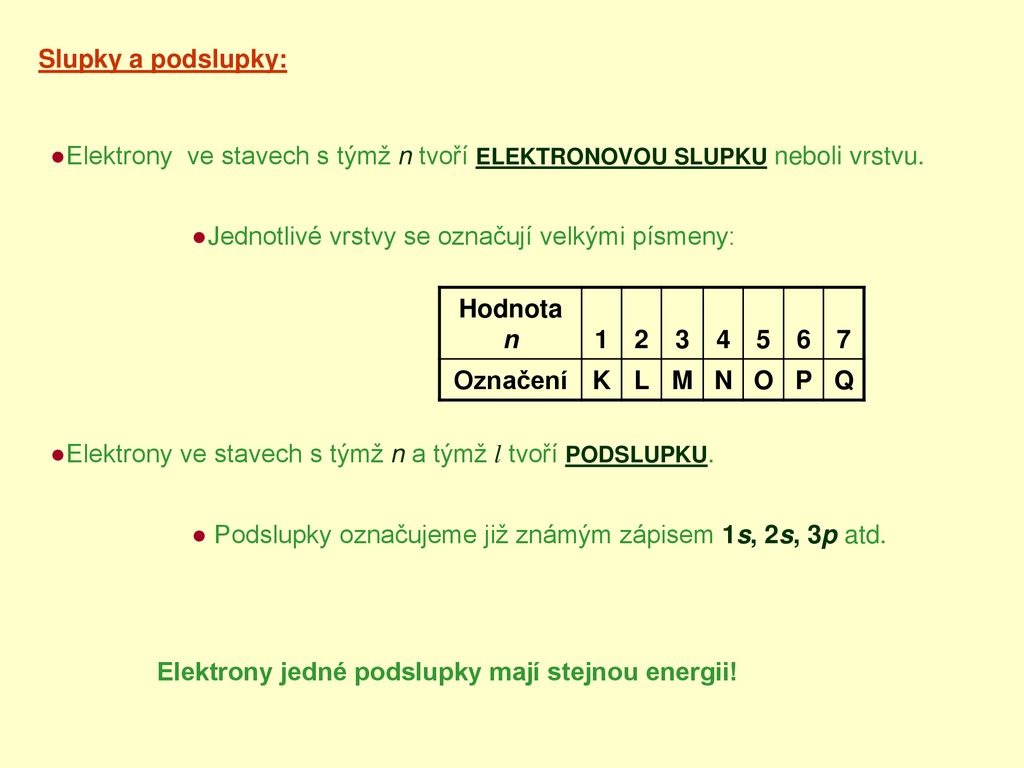
Pravidlo : Orbitaly se zaplňují v pořadí rostoucí hodnoty součtu . Pokud je možno stejné hodnoty dosáhnout více způsoby, např. obsazuje se napřed orbital s nižším hlavním kvantovým číslem (v tomto případě orbital 3d).S protonovým číslem souvisejí tyto termíny: Tři izotopy vodíku s protonovým číslem 1: * Protium obsahuje jeden proton a jeden elektron * Deuterium jeden proton, jeden neutron a jeden elektron * Tritium jeden proton, dva neutrony a jeden elektron Neutronové číslo (N) – je počet neutronů v jádře atomu.se značí n, vyjadřuje energii elektronu. Nabývá hodnot 1 až 7. Orbitaly, které mají stejné hlavní kvantové číslo, tvoří jednu elektronovou vrstvu. Atomy dosud známých prvků obsazují elektrony 7 elektronových vrstev, které se označují čísly 1 až 7 nebo písmeny K,L,M,N,O,P,Q.
Atomy dosud známých prvků obsazují elektrony 7 elektronových vrstev, které se označují čísly 1 až 7 nebo písmeny K,L,M,N,O,P,Q. Maximální počet elektronů v každé vrstvě se rovná dvojnásobku počtu orbitalů, protože v jednom orbitalu mohou být maximálně dva elektrony.
Kolik elektronů je ve valenční vrstvě : Chemická vazba. Zaplněná valenční slupka má osm elektronů. Tento stav se nazývá elektronový oktet. V periodické tabulce prvků objevené D. I.
Jak jdou za sebou orbitaly : Orbitaly se obsazují podle rostoucí energie v pořadí: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p, … S tímto pořadím zcela koresponduje uspořádání prvků v periodickém systému.
Kolik má vodík elektronů
Klasický atom vodíku (někdy nazývaný protium) je tvořen jedním protonem a jedním elektronem.
Atom vodíku 1H je nejjednodušším atomem periodického systému tvořený jedním protonem a jedním elektronem. Je prvkem s-bloku, kde spolu s heliem představují jediné dva nekovové prvky. Vedle 1H má dva další izotopy – deuterium 2H resp.Orbitaly se obsazují podle rostoucí energie v pořadí: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p, … S tímto pořadím zcela koresponduje uspořádání prvků v periodickém systému.
Co je v obalu atomu : je vnější část atomu obklopující atomové jádro. Obal atomu je tvořen elektrony a má záporný náboj.